[h] Reaktionstyper och reaktionsmekanismer
[i] REAKTIONSTYPER OCH REAKTIONSMEKANISMER
Niklas Dahrén, kemilektioner.se
[q] Vilken är reaktionstypen?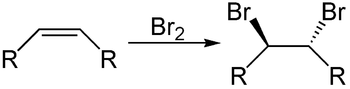
[a] Additionsreaktion
[q] I denna reaktion bildas nästan enbart den ena av
produkterna. Vilken?
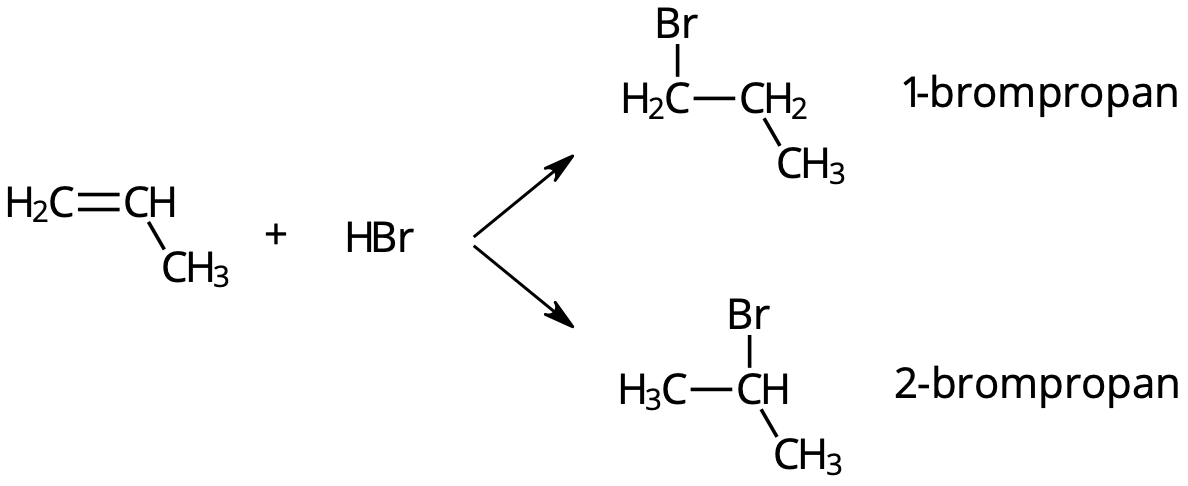
[a] 2-brompropan
[q] Vilken är reaktionstypen?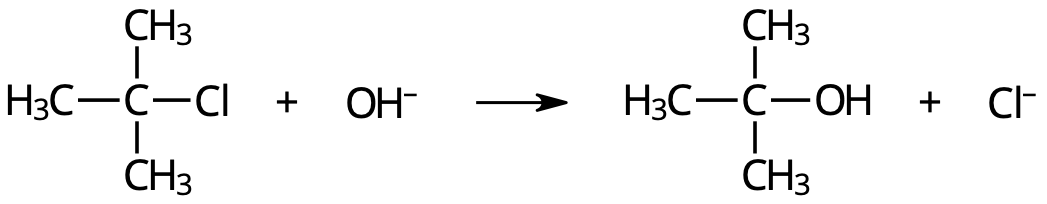
[a] Substitutionsreaktion
SN1
[q] Vilken är reaktionstypen?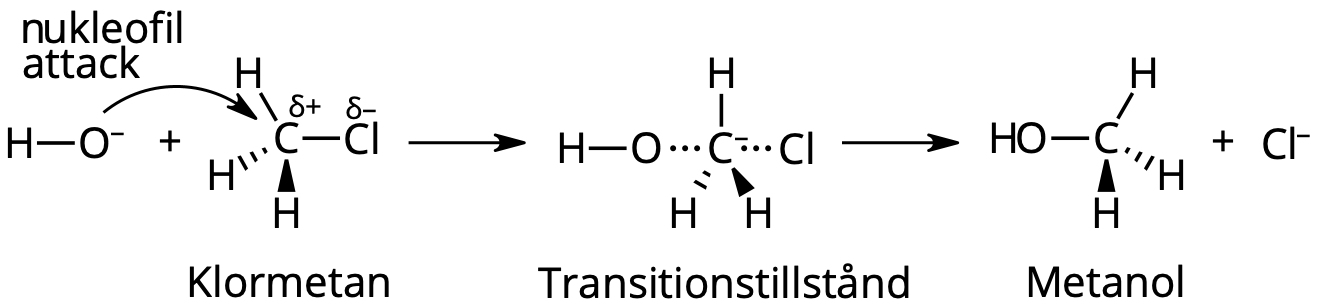
[a] Substitutionsreaktion
SN2
[q] Vilken är reaktionstypen?
[a] Additionsreaktion
[q] Vilken typ av karbokatjon syns på bilden?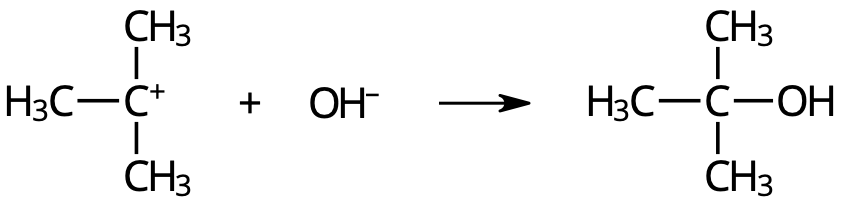
[a] Tertiär karbokatjon
[q] Detta är steg 2 i en typ av reaktion som kallas för...?
[a] Substitutionsreaktion
SN1
[q] Vilken är reaktionstypen?![]()
[a] Substitutionsreaktion
SN1
[q] Nukleofiler
[a] Nukleofiler ("kärnälskare") är ämnen (molekyler eller joner) som attraheras av positiv laddning. Nukleofiler har minst ett fritt elektronpar (alt. en dubbel eller trippelbindning) och är också ofta negativt laddade p.g.a. att de har fått ett elektronöverskott. Det fria elektronparet kan de använda för att ”attackera” och skapa bindningar till fullständigt eller partiellt positivt laddade ämnen, s.k. elektrofiler.
[q] Vilken är reaktionstypen?
[a] Substitutionsreaktion
SN1
[q] Vilken är reaktionstypen?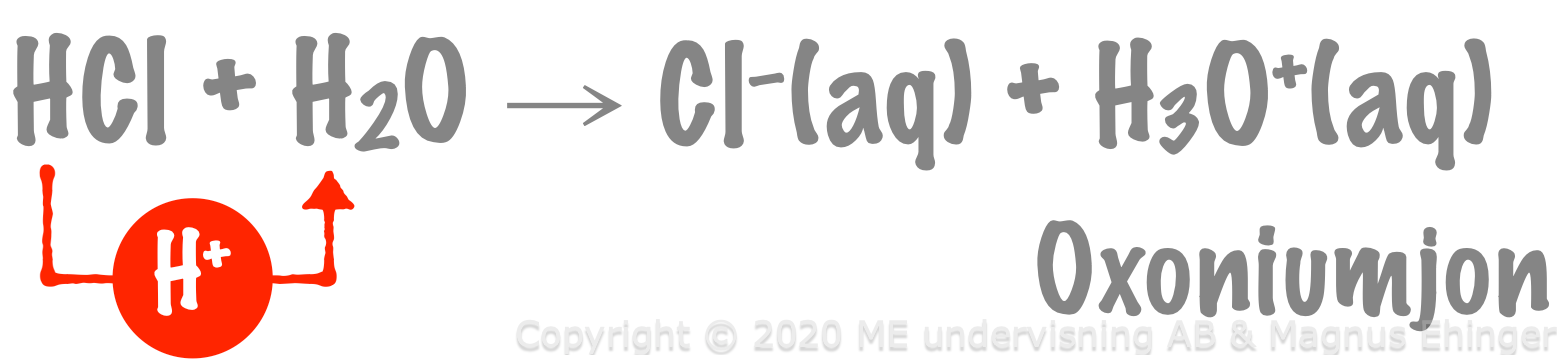
[a] Syra-basreaktion (protolysreaktion)
[q] Elektrofiler
[a] Elektrofiler (”elektronälskare”) är ämnen (molekyler eller joner) som attraheras av negativ laddning. De attraheras av ämnen som har fria elektroner och extra mycket om ämnet har ett elektronöverskott så att en negativ laddning uppstår. Elektrofilerna består av eller innehåller atomer som är fullständigt eller partiellt positivt laddade eftersom atomerna har fått ett elektronunderskott.
[q] Karbokatjoner
[a] En karbokatjon är en positivt laddad jon med laddningen koncentrerad på en kolatom. Karbokatjoner uppkommer som intermediärer (övergångsprodukter/mellansteg) i organiska reaktioner. De är mycket reaktiva p.g.a. den starka positiva laddningen och har därför väldigt kort livstid. Karbokatjoner kan fungera som elektrofiler eftersom de har en positivt laddad kolatom.
[q] SN1-reaktion
[a] SN1-reaktioner:
SN: Nukleofil substitutionsreaktion (S = Substitutionsreaktion, N = Nukleofil attack).
1: Detta är en s.k. monomolekylär reaktion där enbart den ena av de två reaktanterna (ej nukleofilen) deltar i det hastighetsbestämmande första reaktionssteget (totalt är det två reaktionssteg vid en SN1-reaktion).
Reaktionsmekanism: Reaktionen sker i 2 steg. I steg 1 lossnar den lämnande gruppen (halogenen) i form av en negativ jon och det skapas en karbokatjon, i steg 2 attackerar nukleofilen karbokatjonen och skapar en bindning.
[q] SN2-reaktion
[a]
SN2-reaktioner:
SN: Nukleofil substitutionsreaktion (S = Substitutionsreaktion, N = Nukleofil attack).
2: Detta är en s.k. bimolekylär reaktion där båda reaktanterna deltar i det hastighetsbestämmande reaktionssteget (vilket också är det enda reaktionssteget som sker vid en SN2-reaktion).
Reaktionsmekanism: Reaktionen sker i 1 steg. Nukleofilen attackerar elektrofilen (halogenalkanen) bakifrån och börjar skapa en bindning, samtidigt som den lämnande gruppen (halogenen) lossnar framtill i form av en negativ jon.
[q] Vilken typ av karbokatjon bildas som intermediär i denna reaktion?
[a] En primär karbokatjon
[q] Vilken typ av karbokatjon bildas som intermediär i denna reaktion?
[a] En tertiär karbokatjon
[q] Vilken typ av substitutionsreaktion kan ske med denna molekyl?
[a] SN1 p.g.a. ett tertiärt kol (steriskt hinder)
[q] Vilken typ av substitutionsreaktion sker lättast med denna molekyl?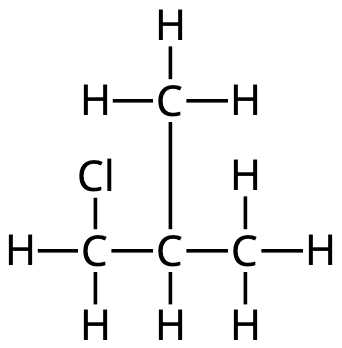
[a] SN2 p.g.a. ett primärt kol (litet steriskt hinder)
[q] σ-bindning (sigma-bindning)
[a] Varje dubbelbindning består av en sigma-bindning (σ-bindning) samt en pi-bindning (π-bindning). De 2 elektronerna i sigmabindningen kallas för sigma-elektroner medan de 2 elektronerna i pibindningen kallas för pi-elektroner. OBS: Vanliga enkelbindningar är alltid sigma-bindningar.
σ-elektronerna befinner sig mellan atomkärnorna och attraheras där starkt av atomkärnorna. Detta skapar en stark bindning som kräver mycket energi för att bryta. Sigma-elektronerna sitter hårt fast och har därför svårt att reagera och skapa bindningar till andra ämnen.
[q] π-bindning (pi-bindning)
[a] Varje dubbelbindning består av en sigma-bindning (σ-bindning) samt en pi-bindning (π-bindning). De 2 elektronerna i sigmabindningen kallas för sigma-elektroner medan de 2 elektronerna i pibindningen kallas för pi-elektroner. OBS: Vanliga enkelbindningar är alltid sigma-bindningar.
π-elektronerna i π-bindningen har blivit repellerade av σ-elektronerna och befinner sig därför inte mellan atomkärnorna utan rör sig snarare ovanför och nedanför atomkärnorna. Dessa elektroner attraheras därmed inte lika mycket av atomkärnorna, sitter lösare och kan därför lättare reagera och skapa bindningar till andra ämnen.
[q] Reaktionen mellan propen och vätebromid är en...?
[a] Additionsreaktion (propen har en dubbelbindning)
[q] Markovnikovs regel
[a] Markovnikovs regel:Vid addition av en vätehalogenid/vätehalid eller av vatten till en alken kommer vätet hamna på den kolatom vid dubbelbindningen som redan binder flest antal väten (halogenen, eller OH-gruppen om det gäller vatten, hamnar därför på den kolatom vid dubbelbindningen som binder minst antal väten).
Markovnikovs regel (lite annorlunda uttryckt):
Vid addition av en vätehalogenid/vätehalid eller av vatten till en alken kommer vätet placeras på den plats som ger upphov till den mest stabila karbokatjonen.
[q] Förklara reaktionsmekanismen vid nedanstående reaktion och varför det i praktiken nästan enbart är den ena produkten som bildas!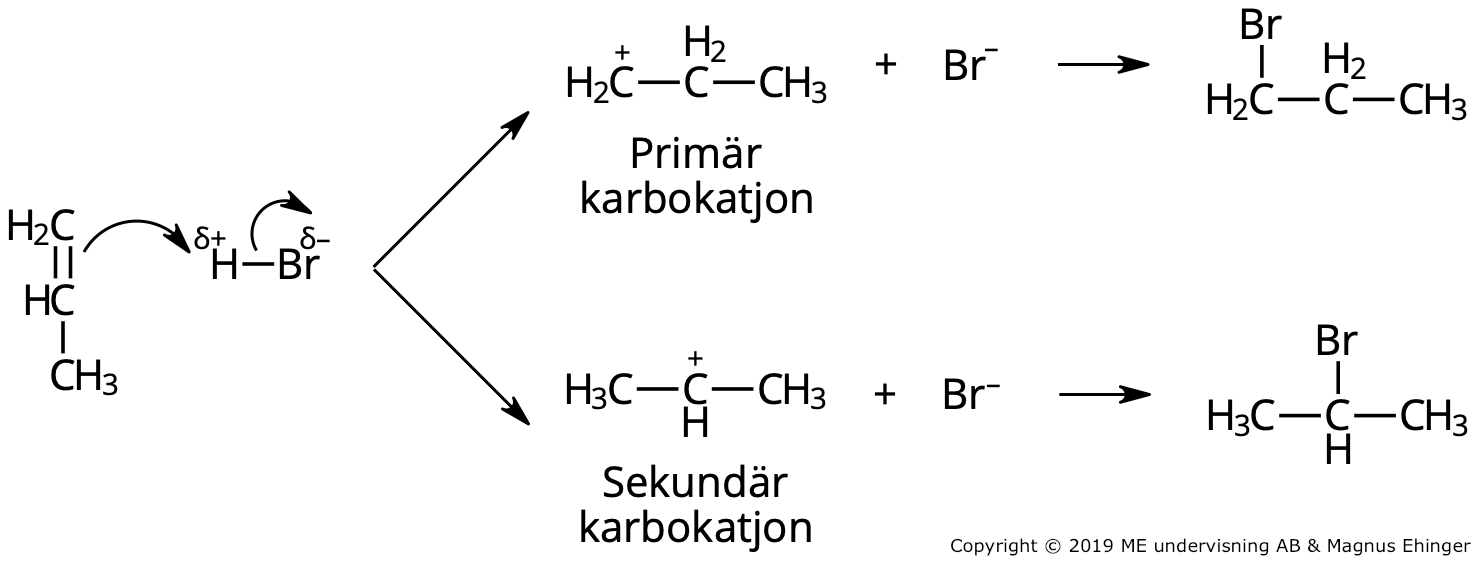
[a] Steg 1 - En karbokatjon bildas: Propen är en nukleofil p.g.a. pi-elektronerna i dubbelbindningen. Vätejonen/protonen som avges från vätebromid fungerar samtidigt som en elektrofil. Pi-elektronerna i dubbelbindningen hos propen skapar en bindning till protonen. Det skapas då alltså en bindning mellan protonen och en av kolatomerna i propen. Propen har nu blivit en karbokatjon.
Steg 2 - En nukleofil attack sker på karbokatjonen:
Produkten som bildas är i stort sätt enbart 2-brompropan. Anledningen är att sekundära karbokatjoner är mer stabila/mindre reaktiva än primära. Det krävs därför mindre aktiveringsenergi för sekundära karbokatjoner att bildas, och det är därför större sannolikhet att dessa bildas. Därför kommer det att bildas nästan enbart 2-brompropan eftersom intermediären då blir en sekundär karbokatjon. För att 1-brompropan ska bildas så krävs det nämligen att en primär karbokatjon bildas som intermediär vilket alltså kräver mer aktiveringsenergi.
[q] Vilken är reaktionstypen?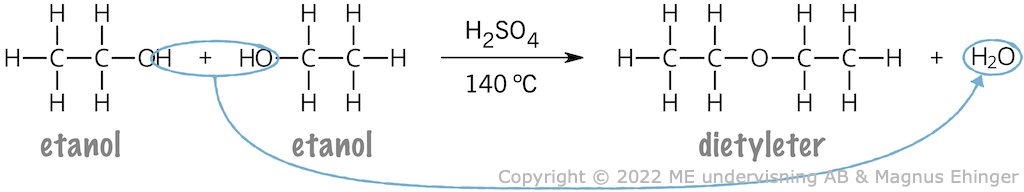
[a] Kondensationsreaktion
[q] Vilken är reaktionstypen?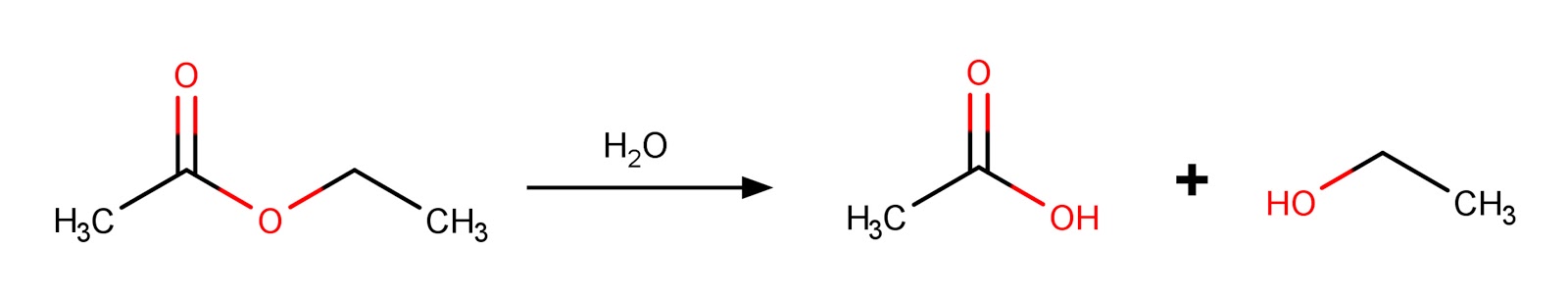
[a] Hydrolysreaktion
[q] Vilken är reaktionstypen?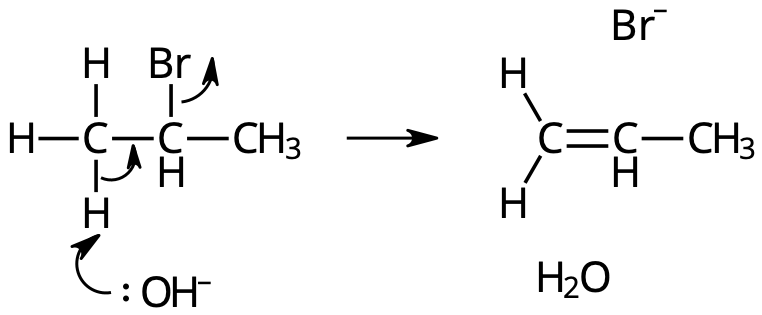
[a] Eliminationsreaktion
[q] Redogör för reaktionsmekanismen bakom estrars kondensationsreaktioner
[a] 
[q] Vilka ämnen behövs vanligtvis för att kunna syntetisera en ester?
[a] En karboxylsyra + en alkohol + en stark syra (katalysator)
[q] Reaktionsmekanism
[a] En reaktionsmekanism beskriver stegvis hur en viss kemisk reaktion går till. Många kemiska reaktioner sker nämligen i flera små steg (delreaktioner) innan de slutgiltiga produkterna bildas.
Reaktionsmekanismen innefattar hur de kemiska bindningarna förändras (vilka gamla bindningar som bryts i reaktanterna och vilka nya som skapas) och hur övergångstillståndet/det aktiverade komplexet uppstår inkl. dess sammansättning/struktur.
Reaktionsmekanismen visar till sist vilka de slutgiltiga produkterna är, inkl. deras struktur, samt hur dessa uppstår.
[x] Niklas Dahrén, kemilektioner.se
[/qdeck]
